该成果以“Direct Electrochemistry of Glucose Dehydrogenase-Functionalized Polymers on a Modified Glassy Carbon Electrode and Its Molecular Recognition of Glucose”为题发表于International Journal of Molecular Sciences(中科院二区TOP, IF: 6.208)杂志。

Introduction
迄今研究人员已经开发了许多分析方法对于葡萄糖的检测,其中包括高效液相色谱、光电化学方法、比色法和电化学分析技术。电化学生物传感器以其特异、高效、简便、快速等特点在生物、医学和工业分析中得到了广泛的应用。为了提高检测的准确性和可靠性,介体型葡萄糖氧化酶传感器最早被开发,并在体外电子受体上进行了测试。然而,它的酶促反应高度依赖于作为电子受体的溶解氧浓度。相比之下,葡萄糖脱氢酶(GDH)被认为是最有希望取代葡萄糖氧化酶的酶,因为它不使用氧作为电子受体,避免了氧气干扰带来的误差。
本研究采用GDH作为识别单元,将其固定于胺化聚乙二醇(mPEG)、羧酸官能化多壁碳纳米管(fMWCNTs)、以及离子液体(IL)复合功能聚合物修饰玻碳电极(GCE)上,所构建的电极表示为NF/IL/GDH/mPEG-fMWCNTs/GCE。mPEG中的氨基以及fMWCNTs和IL中的羧基具有更好的协同作用,从而更有效地调节复合功能聚合物膜的疏水性、稳定性、电导率和生物相容性。此外,还研究了GDH在改性GCE上的电化学行为。该复合功能聚合物可以保留GDH的构象结构和催化活性,从而构建了高灵敏度、高稳定性和高选择性的葡萄糖识别和检测生物传感器。
Results and Discussion
1. 不同改性电极的电化学行为研究
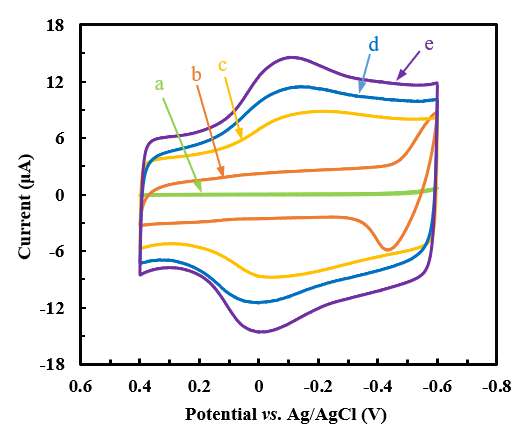
Figure 1. Cyclic voltammograms (CVs) of different modified GCEs. (a) bare GCE, (b) NF/fMWCNTs/GCE, (c) NF/mPEG-fMWCNTs/GCE, (d) NF/GDH/mPEG-fMWCNTs/GCE, and (e) NF/IL/GDH/mPEG-fMWCNTs/GCE. The experiments were conducted in a sodium phosphate-buffered saline (PBS) solution (50 mM, pH 7.0) versus Ag/AgCl. at scan rate of 0.05 V s−1, 25 ± 1 °C.
逐层滴加纳米修饰材料,通过循环伏安法进行探究不同材料修饰电极表面上的循环伏安法信号特征。从图1可以看出,裸玻碳电极(曲线a)在没有任何材料修饰的情况下没有响应电流且无特征氧化还原峰。其中NF/IL/GDH/mPEG-fMWCNTs/GCE(曲线e)的信号最好。fMWCNTs的加入显著增加了工作电极处的电流信号,但其仅有氧化响应信号,没有回扫信号(曲线b),仅有fMWCNTs修饰在电极表面不会呈现出可逆的电化学行为。mPEG的加入提高了电化学信号(曲线c),未加入GDH时材料本身的形式电位(Eo'=Epa/2+Epc/2)为-124 mV。NF/GDH/mPEG-fMWCNTs/GCE(曲线d)和NF/IL/GDH/mPEG-fMWCNTs/GCE对应的形式电位vs. Ag/AgCl分别为-61 mV,其特征是GDH将葡萄糖吸附在电极表面。可以作为电解质的载体的IL的加入并不会改变电势,促进蛋白质向电极的直接电子传递。加入GDH之后信号随之增强,是因为GDH本身是一种电活性物质,加入GDH会导致响应电流增大,此外选择的纳米材料本身具有巨大的比表面积,能为负载葡萄糖脱氢酶提供更多的载点,同时纳米材料缩短了电极表面到酶活性中心的电子传递路径,响应电流信号增大。将IL修饰在电极表面后可为GDH固定在纳米材料的提供良好的反应微环境,从而与mPEG协同增强修饰电极的催化活性。这一结论得到了IL能够显著增强直接效应的结果的支持。阳极峰电流与阴极峰电流之比(Ipa/Ipc≈1)表明改性电极的电化学过程为准可逆过程。此外,NF/IL/GDH/mPEG-fMWCNTs/GCE的响应信号比其他复合材料更强,因此可以用于后续的电化学研究。mPEG中的氨基和MWCNTs中的羧基的存在有助于将mPEG-fMWCNTs均匀分散在功能膜中提高电极的电化学性能,而Nafion的存在提供了良好的微环境保护了电极,增强其稳定性。
2. 不同扫描速度对NF/GDH/IL/mPEG-fMWCNT/GCE电极的影响
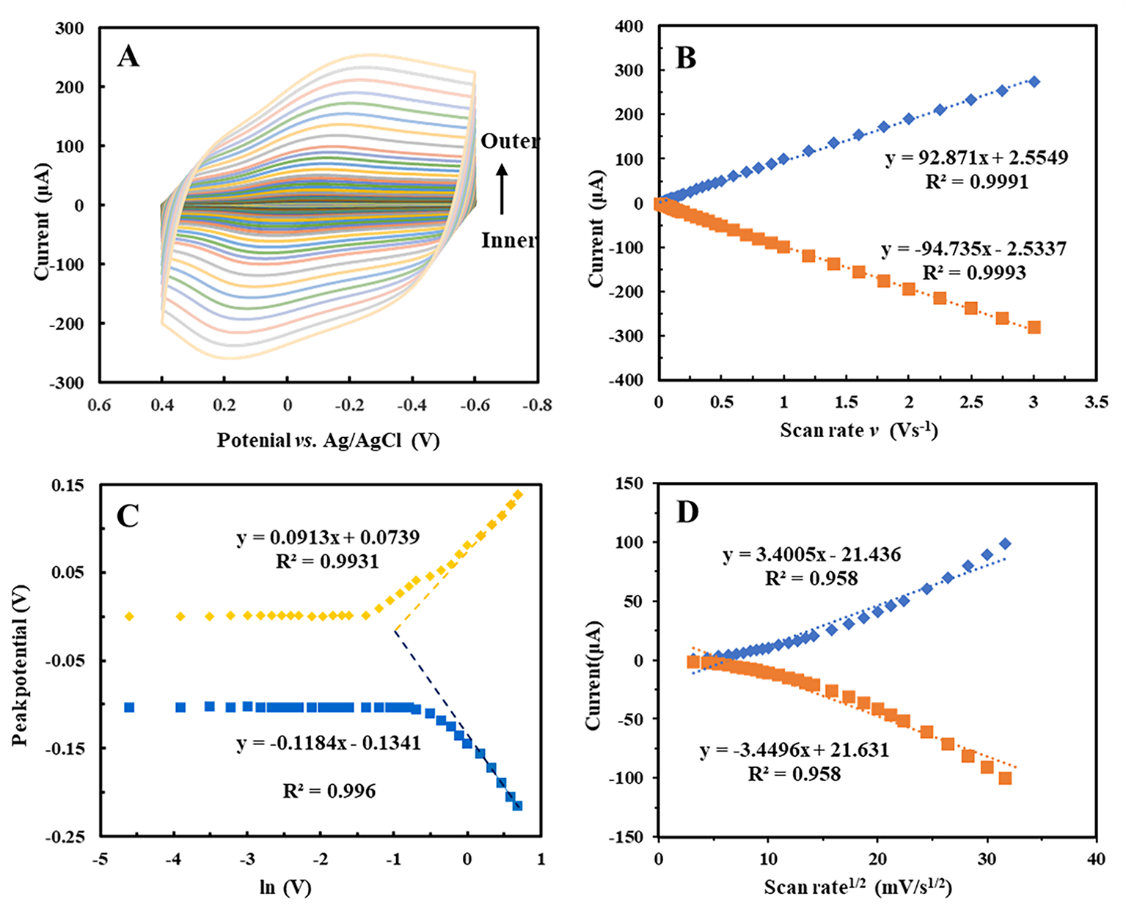
Figure 2. (A) CVs of the NF/GDH/IL/mPEG-fMWCNTs-modified GCE at different scan rates. (B) Plot of peak current (Ip) versus scan rate (υ). (C) Plot of peak potential (Ep) versus lnυ. (D) Plot of peak current versus scan rate1/2. The experiments were conducted in a PBS solution (50 mM, pH 7.0) versus Ag/AgCl. at 25 ± 1 °C.
电化学参数随着扫速的增加而产生变化。图2 A为扫速为0.1-3 V s-1时的循环伏安曲线。采用循环伏安法研究了修饰电极的电化学行为,阳极和阴极的峰值电流随着扫描速度的增加呈现一定的比例变化。从图2 B可以看出,在0.1-3 V s-1扫描速率范围内,线性度有所提高,对响应电流进行回归分析,回归方程如下:Ipa(μA) = −94.735v (V s−1) – 2.5549,R2 = 0.9993;Ipc (μA) = 92.871v (V s−1) + 2.5549,R2 = 0.9991。这表明氧化还原反应是一个表面控制的电化学过程,氧化还原信号来源于固定在fMWCNTs层上的GDH。这一结果表明电极过程主要受动力学反应控制。
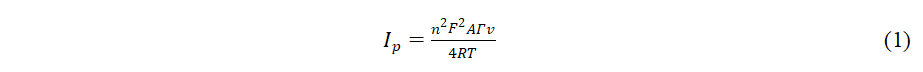
根据峰电流( Ip )对扫描速率υ的斜率,A为修饰电极的表面积: 0.07065 cm2。GDH电活性中心在GCE表面的平均表面浓度( Γ )为4.04 × 10-10 mol cm-2,而基于GDH ( PDB ID: 1gco ,直径约10 nm)的PDB数据的理论Γ值为1.7 × 10-10 mol cm-2。与裸玻璃电极相比,交联载体mPEG和fMWCNTs的亲水表面更容易形成致密的GDH分子阵列。随着扫描速度的增加,峰值电压也受到影响。当扫描速度足够大时,自然对数与峰值电压呈线性关系。峰电位在1.2 ~ 2 V s-1范围内,通过Epa = -0.1184ln(V) -0.1341 R2 = 0.996和Epc = 0.0913ln(V) + 0.0739 R2 = 0.9931研究这些方法的线性(图2 C )。
根据Laviron’s的方程:
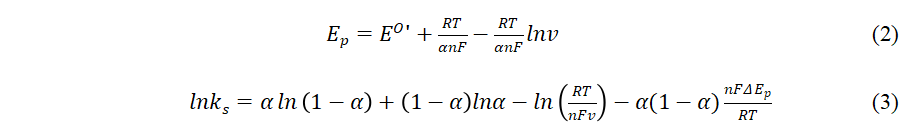
其中α为阴极电子转移系数( 0.3 < α < 0.7),n为电子数,T为温度:293 K,R为气体常数:8.314 J K-1mol-1,F为法拉第常数:96,485 Cmol-1。
因此,改良修饰电极的阴极电子转移系数( α )、表观异相电子转移速率常数( ks )值和电子数( n )分别为0.5、6.5 s-1和2。通过对根号扫速的自然对数与峰值电流的关系进行分析(图2D),发现根号扫速与峰值电流的线性关系较差,说明在该修饰体系中电子的转移受动力学控制,而非扩散控制。
3. 不同pH对NF/GDH/IL/mPEG-fMWCNT/GCE电极的影响
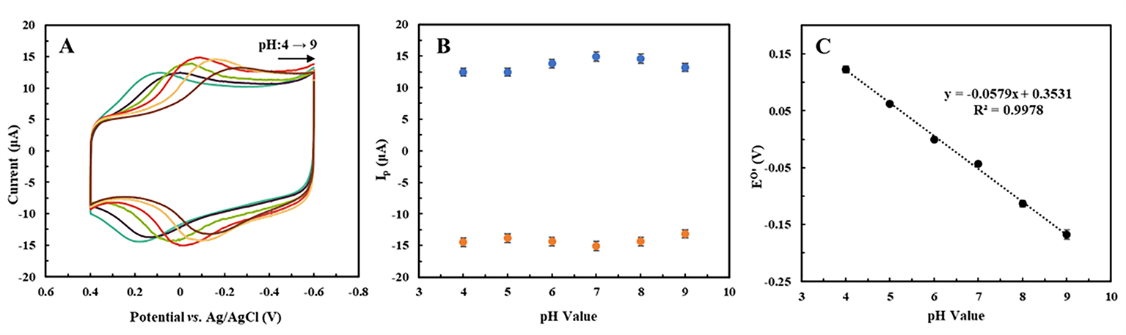
Figure 3. (A) CVs of the NF/GDH/IL/mPEG-fMWCNTs in 50 mM PBS at different pH values (from left to right): 4.0, 5.0, 6.0, 7.0 8.0 and 9.0, respectively. (B) Plot of peak current ratios versus pH values. (C) Plot of formal potential Eo′ versus pH values. versus Ag/AgCl. scan rate of 0.05 V s−1, 25±1°C.
通过循环伏安法(CV)探究了NF/IL/GDH/mPEG-fMWCNTs/GCE在不同pH值下的电化学行为,测试环境中PBS溶液的pH影响修饰电极的电化学过程。图3A显示了该电极在pH为4-9的PBS溶液中的峰电流。图3B显示,随着pH值的增加,测得的氧化峰和还原峰的位置向负电压方向移动。当pH从4变化到7时,峰值电流增大,当pH从7增加到9时,峰值电流减小,在pH为7时获得最大阴极电流,同时在该条件下阴阳极峰值电流比更接近于1。在后续的研究中,选择pH为7.0作为最适pH。此外,从pH 4到 9时,形式电位与pH呈线性关系(图3C)。该斜率为57.9 mV pH-1,接近Nernstian值59.2 mV pH-1。这些结果同样表明电子在该电化学体系中的直接电化学行为是可逆的。
4. 构建的生物传感器对葡萄糖分子的识别响应
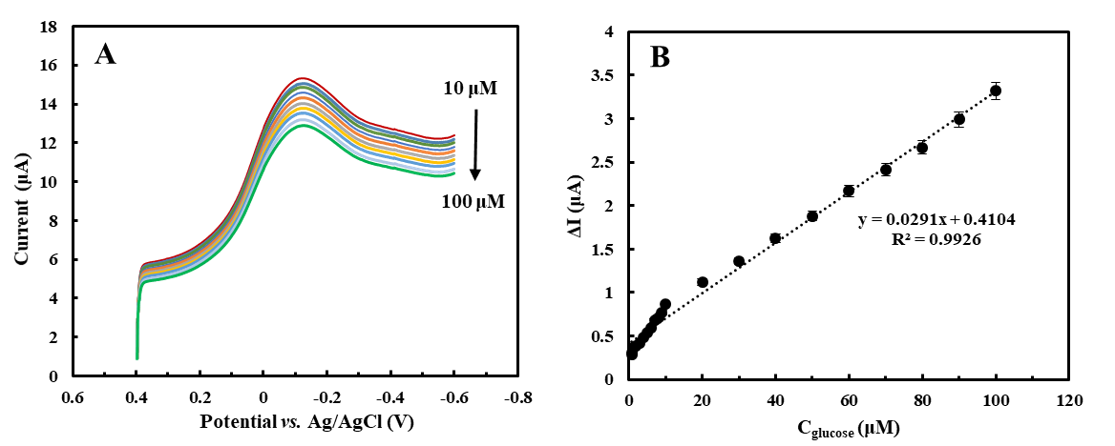
Figure 4. (A) Linear sweep voltammograms (LSVs) of the NF/GDH/IL/mPEG-fMWCNTs electrode-modified GCE in the presence of different concentrations of β-D-glucose (10, 20, 30, 40, 50, 60, 70, 80, 90, and 100 μM). (B) Linearity of peak current difference (ΔI) versus glucose concentration. The experiments were performed in PBS (50 mM, pH 7.0) at a potential of −124 mV versus Ag/AgCl at 25±1°C.
线性扫描伏安法(Linear sweep voltammograms, LSV)是检测物质的常用方法。图4A显示了50 mM, pH 7.0 PBS环境中,在室温条件下NF/IL/GDH/mPEG-fMWCNTs/GCE在无或存在不同浓度葡萄糖(0.8~100μM)时的LSV图,检测电位为-61 mV vs Ag/AgCl。随着反应的进行,峰值信号逐渐衰弱,这是因为葡萄糖的逐渐加入导致修饰在玻碳电极表面上的GDH减少,进而导致峰电流的降低。
表观米氏活性(km)表示生物传感器的酶-底物动力学:
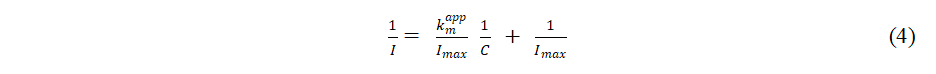
式中,I为稳态电流,Imax为稳态底物条件下的最大电流,km为表观米氏常数,C为葡萄糖浓度。Imax和km值由图4 B所示的图外推得到。这是因为在检测过程中,低至0.21 mM的km显示出较强的底物结合能力和对葡萄糖的高亲和力。所选复合纳米材料可以减小GDH与GCE之间的桥联距离。
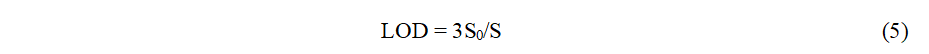
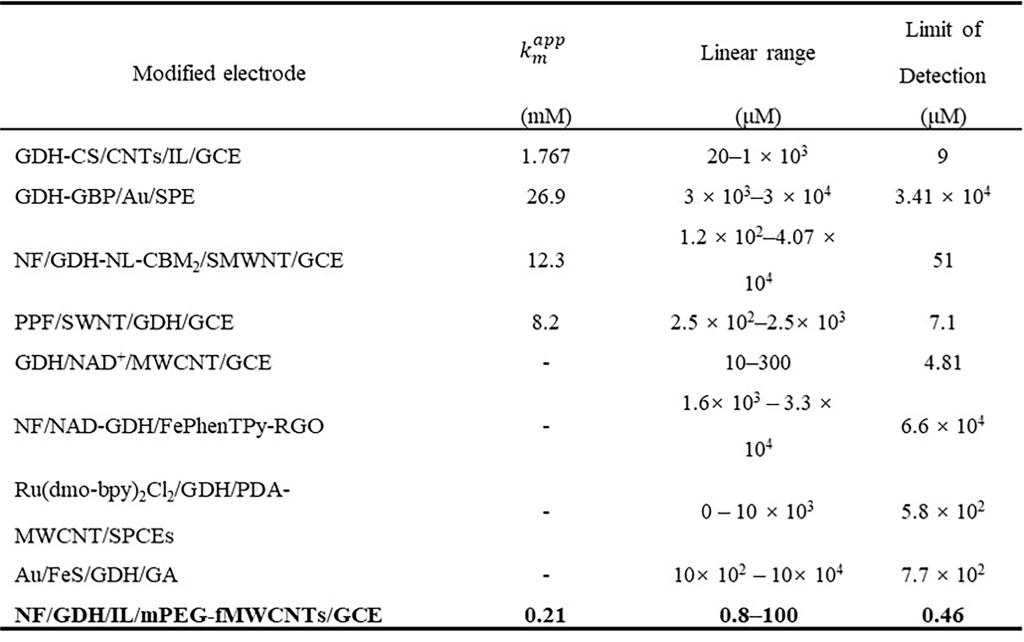
其中S0和S分别表示空白溶液下测得的标准偏差和线性范围曲线的斜率。利用公式(5)计算出检测限为0.46 μM,这与最近研究报道的GDH生物传感器相比,所提出的生物传感器的显著优势如表1所示。
Table 1 Comparison of several glucose dehydrogenase biosensors
5 所构建的传感器与HPLC对葡萄糖检测比较
葡萄糖使用浓度为10、20和50 μM。检测前,含葡萄糖注射液经0.22 μm微孔滤膜过滤除去杂质。葡萄糖样品分别通过HPLC和电化学传感器进行检测。在电化学工作站上记录稀释后的葡萄糖注射液的峰电流和线性伏安曲线。
葡萄糖(纯度99%)用5 mM葡萄糖混合标准溶液的稀硫酸溶液配制。通过标准曲线将获得的峰面积转换为浓度,HPLC检测线性范围为0.36~18 μg mL-1,线性方程为y = 1707.8C(μg mL-1) - 177.7。
实验结果如表2所示:
Table 2 Sample determination by HPLC and electrochemical sensor methods (n = 3)

实验结果表明,所构建的电化学传感器在检测目标分子时具有较高的准确性和精确度。相比于传统的高效液相色谱法,该传感器避免了繁琐的样品制备过程和昂贵的测试设备要求,使得分析过程更加便捷和经济。
6. NF/mPEG-fMWCNTs/IL/GDH/GCE的抗干扰性研究

Figure 5. Anti-interference ability of NF/GDH/IL/mPEG-fMWCNTs/GCE in 50 mM pH 7 PBS at 25 ± 1 °C.
采用安培电流-时间(I-t)法考察了修饰电极NF/GDH/IL/mPEG-fMWCNTs/GCE的抗干扰能力。当将潜在的干扰物质蔗糖、乳糖、乙醇、丙醇和乳酸浓度分别加入检测液中,浓度均为200 μM,其响应电流并未出现显著的变化(图5)。然而,当再加入浓度为10 μM的葡萄糖时,电化学传感器显示了相应的电流信号。更进一步地,当加入浓度为100 μM的葡萄糖时,强烈的信号响应被检测到。这些结果表明,我们建立的电化学传感器具有良好的选择性和抗干扰性。这也彰显了酶作为识别元件的优势,因为酶的选择性高以及极高的灵敏度使得它能够直接在复杂样品中完成对于葡萄糖的检测。
Conclusion
总之,我们提出了一种基于Nafion、IL、MPEG、FMWCNT和GDH复合修饰玻碳电极的葡萄糖检测策略。用循环伏安法、紫外-可见分光光度法、荧光光谱法、电化学阻抗谱法、扫描电镜对复合聚合物膜进行了表征,在本研究中,GDH在修饰的GCE上的电子转移常数(ks)为6.5 s-1,这是一个可以快速检测葡萄糖分子的水平。对于0.8 μM-100 μM范围的葡萄糖识别具有良好的响应,LOD=0.21 μM。对于市售葡萄糖注射液的检测,我们将电化学传感器和高效液相色谱法进行了比较,该传感器显示出良好的准确性和简便性。基于葡萄糖脱氢酶传感器灵敏度高、抗干扰性强、贮存时间稳定等特点,为葡萄糖脱氢酶传感器今后在血糖测量、食品安全、发酵工程等方面的应用提供了新的思路。
原文链接:https://doi.org/10.3390/ijms24076152